


近日,《自然》杂志子刊《自然 · 生物医学工程》(Nature Biomedical Engineering)上报道了药学院顾臻教授团队的一项研究。团队开发了一种基于“细胞仓库”(cell reservoir)的免疫细胞局部缓控释技术,在动物模型上验证了该技术能显著增强CAR-T细胞抗实体瘤的疗效。

针对实体瘤复发
手术是现代临床上用于治疗肿瘤患者的主要选择,但是术后的肿瘤复发和肿瘤的转移仍是导致癌症病患死亡的主要原因。在实体瘤的手术切除中,由于缺乏精准的影像技术导航,通常临床医生会切除大于实际肿瘤体积的组织。即便这样,由于很多肿瘤细胞具有较强的浸润性和侵袭性,手术很难完全清除所有的肿瘤细胞。即使辅助化疗或放疗等治疗手段,这些残余的癌细胞仍然会在术后卷土重来。
近些年来肿瘤免疫治疗成为临床肿瘤治疗的有效手段,取得了令人振奋的治疗效果。CAR-T细胞作为“明星”疗法,在血液肿瘤的治疗中取得了巨大成功。美国FDA已经批准了五款CAR-T细胞疗法用于治疗B细胞淋巴瘤等血液与多发性骨髓瘤。然而CAR-T细胞疗法在治疗实体瘤上却遇到了很多的挫折,这在很大程度是由于实体瘤的生理屏障及肿瘤微环境的免疫抑制特性,抑制了CAR-T细胞的活性和生存率。
可植入“细胞仓库”
那有什么方法能够维持CAR-T细胞在肿瘤微环境的活性,发挥CAR-T细胞对实体肿瘤的杀伤能力呢?先前的很多研究指出,直接在肿瘤部位批量注射的CAR-T细胞会很快丧失活性并死亡。同时,除了肿瘤免疫抑制微环境,肿瘤细胞本身也可以通过免疫检查点抑制通路去逃逸T细胞的识别功能并抑制其杀伤能力。
基于这个思路,研究人员设计了一种基于“细胞仓库”的细胞局部缓控释技术,将两种不同类型的细胞(CAR-T细胞和抗PD-L1抗体修饰的血小板)和包载IL-15细胞因子的纳米颗粒同时装载进一个生物相容性较好的可植入水凝胶中,通过水凝胶的缓释能力实现CAR-T 细胞的可控释放,避免快速释放导致的CAR-T细胞大量失活,并通过IL-15的作用维持CAR-T细胞活性。同时在术后的炎症环境中,表面修饰了PD-L1抗体的血小板能够被激活并释放抗PD-L1的抗体,阻断免疫检查点抑制通路,增强CAR-T细胞的杀伤能力,可更有效地抑制术后的癌症复发。研究人员将该载细胞凝胶称为“细胞仓库”,用作细胞的局部缓控释。这是继2018年的“联合细胞药物递送”治疗急性髓系白血病之后,顾臻团队再次将细胞联合策略用于肿瘤免疫治疗。
细胞协同,抑制术后肿瘤复发
在小鼠实验中,这种细胞递送技术的抗术后肿瘤复发得到了验证。研究人员先在皮下建立了人黑色素肿瘤模型,等到肿瘤长到一定大小后再进行手术切除,模拟临床肿瘤的手术治疗。随后,在肿瘤切除部位植入了装载两种细胞的水凝胶,观察这种细胞递送策略的治疗效果。此外,研究人员设计了不同的对照治疗组,包括生理盐水、直接注射CAR-T细胞和抗PD-L1抗体-血小板、以及装载一种细胞的水凝胶。
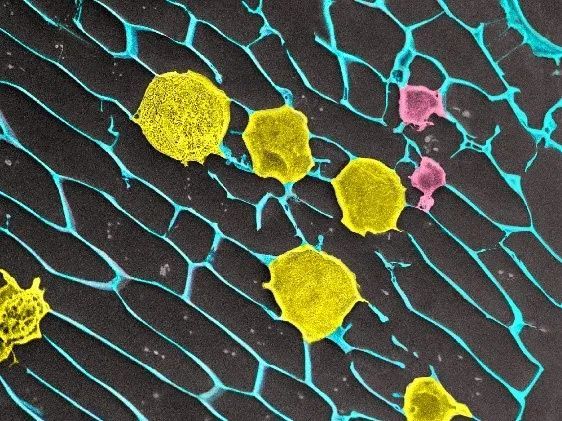
“细胞仓库”递送系统。CAR-T细胞(黄色)和抗PD-L1抗体连接的血小板(紫红色)装载在高生物相容性的透明质酸水凝胶(蓝色)中(图片来源:研究作者提供)。
在治疗3周后,小鼠体内术后复发癌症病灶受到显著抑制。而在多个对照组实验中,肿瘤都无法得到有效抑制,出现复发现象。值得注意的是,跟踪这种细胞联合递药组治疗的肿瘤,其肿瘤荧光强度仅为生理盐水组的1/60,显示出了良好的抑瘤效果。同时,研究人员也验证了CAR-T细胞在术后肿瘤部位的增殖能力,结果显示使用“细胞仓库”递送的CAR-T细胞显示出了良好的增殖能力,然而直接注射的CAR-T对照组则很快丧失活力并死亡。
同时,这种局部的CAR-T递送策略起到了抑制远端肿瘤的疗效。在研究人员构建的双位肿瘤模型中,在一侧的肿瘤进行术后治疗,另一侧的肿瘤也出现了体积缩小的现象,证明局部递送的CAR-T细胞也聚集到了远端的肿瘤,为抑制术后的肿瘤转移提供了可能。
总结
本研究通过一种“细胞仓库缓控释”的递送策略,将CAR-T细胞和抗PD-L1抗体连接的血小板装载在水凝胶中,通过缓慢释放CAR-T细胞并阻断免疫检查点通路提升CAR-T细胞对肿瘤的杀伤力,对抑制术后癌症复发起到了良好的治疗效果。顾臻教授及研究人员指出,一方面这还可以和其他疗法(例如化疗放疗)联合使用,更好的抑制肿瘤复发和转移;同时,新型细胞递送策略也为其他细胞疗法和相关疾病的治疗提供了新思路。