


2017年11月3日,美国化学会权威期刊《ACS Central science》在线发表了侯廷军教授课题组题为《Combating Drug-Resistant Mutants of Anaplastic Lymphoma Kinase with Potent and Selective Type‑I1/2 Inhibitors by Stabilizing Unique DFG-Shifted Loop Conformation》的研究论文。该研究报道了一类新型的抗耐药性间变性淋巴瘤激酶(ALK)“桥联”小分子,该类抑制剂可扩展结合到ALK疏水性的背部口袋,体外活性优于FDA已上市药物克唑替尼和色瑞替尼,也是目前已报导的体外活性最强的Type‑I1/2型ALK抑制剂(001-017:IC50= 0.27 nM)。
ALK蛋白是一种受体酪氨酸激酶,是胰岛素受体超家族中的一员,它的过度表达可与多种基因发生重排融合而被激活,通过自体磷酸化实现ALK蛋白活化,激活下游信号转导通路,从而诱导肿瘤的发生与发展。仅仅经过4年的研发,靶向ALK的第一个药物克唑替尼(crizotinib)便被美国FDA批准用于治疗EML4-ALK融合型非小细胞肺癌,其高响应率使它成为最成功的抗癌药物之一。尽管克唑替尼在治疗初期的反应很好,但大部分患者在使用克唑替尼治疗约10个月后会产生耐药,出现了疾病的复发。经过近些年的临床应用,多种类型的ALK耐药突变被陆续发现,如L1196M
、C1156Y、G1269A、G1202R、S1206Y、R1275Q、T1151ins、L1152R、I1171T和F1174L等。因此,设计和开发骨架新颖的ALK抗耐药小分子抑制剂迫在眉睫。
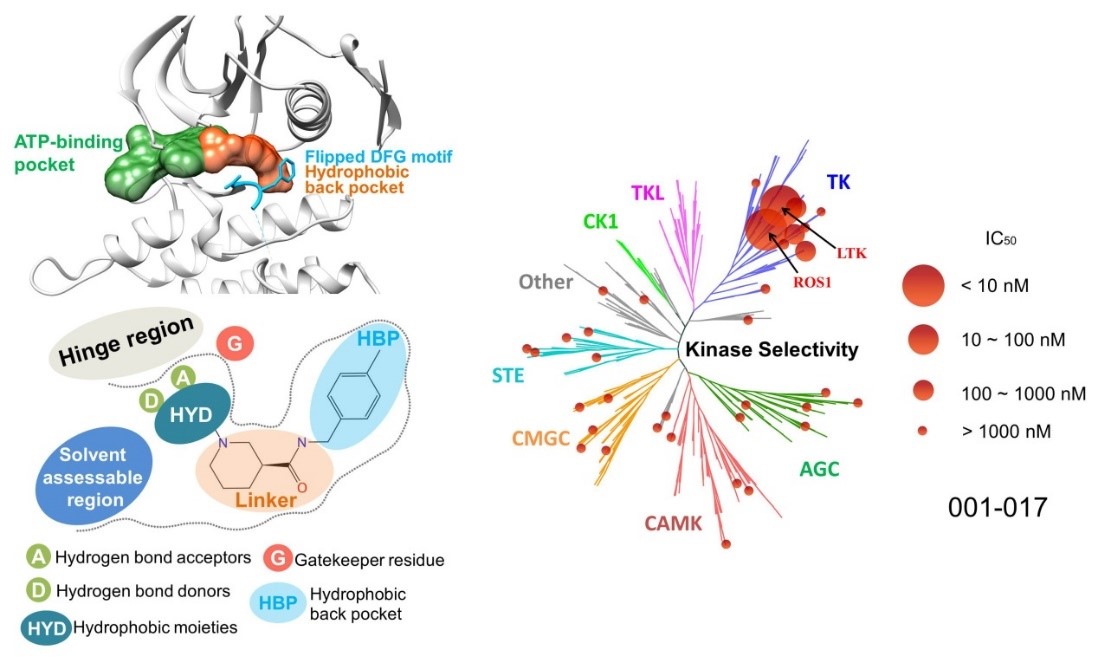
为了克服药物耐药性的问题,侯廷军教授课题组采用多种分子模拟技术设计了一类新型的ALK小分子抑制剂,可同时靶向ATP活性位点和扩展的背部疏水口袋。该类抑制剂在分子层面以及细胞层面均表现出优异的生物活性,较FDA已上市药物克唑替尼和色瑞替尼体外活性更强。其中,最优的一个化合物(001-017)对多种ALK耐药突变体仍表现出很强的抑制活性。此外,针对35种来自不同家族的激酶谱分析显示,001-017化合物具有高度的激酶选择性,因此可能减少由于脱靶效应导致的毒性问题。该研究为开发下一代抗耐药性ALK抑制剂提供了新策略。
浙江大学药学院14级博士研究生潘培辰为该论文的第一作者,浙江大学侯廷军教授和北京大学深圳研究生院黄�教授为该论文并列通讯作者。
全文链接:http://pubs.acs.org/doi/full/10.1021/acscentsci.7b00419